Entropia
A entropia é uma
propriedade extensiva decorrente da segunda lei da termodinâmica, é apenas
função do estado inicial e final de ciclos termodinâmicos, sua unidade é kJ/kg.K
ou kmol/kg.K
e, para sistemas reversíveis, é definida como:
A referência da
entropia, seu valor zero, é, por definição, o valor da entropia na temperatura
zero absoluta. No entanto, algumas tabelas fornecem valores referentes a estados
arbitrários. A variação da entropia
pode ser calculada pela integração da equação anterior desde o estado inicial
até o estado final. Quando isso é feito, a definição do zero de entalpia passa a
ser irrelevante.
Como a entropia é uma
propriedade, a sua variação entre estados independe do caminho que o processo
percorreu para atingir o estado final -2 - a partir do estado inicial -1.
Como os sólidos e líquidos são
incompressíveis, a variação de volume é desprezível e o calor específico pode
ser considerado constante. Desta maneira, as equações de Gibbs podem ser
escritas da seguinte maneira:
Considerando o calor específico constante, a
variação da entropia pode ser calculada da seguinte maneira:
Conforme visto na seção Calor Específico, ele depende da temperatura. Portanto,
se considerarmos uma aproximação linear, a variação da entropia será dada por:
A primeira equação de
Gibbs pode ser escrita da seguinte maneira:
Analogamente, para a
segunda equação de Gibbs, teremos que;
e as seguintes
relações são válidas para gases perfeitos:
Portanto, teremos que:
Para resolvermos estas
equações é necessário conhecer a variação do
calor específico
com a temperatura. Existem três
possibilidades para tratar deste problema: Neste caso, as expressões podem ser integradas
diretamente resultando em:
Neste caso,
considerando uma aproximação linear, teremos
que:
O
erro cometido pela simplificação de considerar o calor específico constante
dependerá das constantes específicas de cada gás e da diferença absoluta de
temperatura no processo.
Em processos
isentrópicos, as expressões
anteriores são iguais a zero e, conseqüentemente, elas podem ser utilizadas para
calcular as pressões e/ou os volumes específicos. Neste caso, teremos também 3 possibilidades: Neste caso teremos
que:
e
No entanto, como visto anteriormente, R=cp0-cv0,
teremos que:
Se definirmos
a relação de calor específico - k - como sendo a relação entre o
calor específico a pressão constante e o calor específico a volume constante,
teremos que:
A última expressão pode ser escrita da seguinte
maneira:
Esta expressão é
válida para todos os processos adiabáticos e reversíveis que envolvem um gás
perfeito com calor específico constante.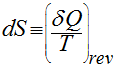
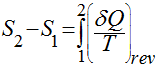
Equações de Gibbs
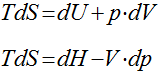
Variação de Entropia em Sólidos e Líquidos
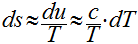
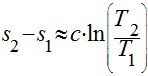
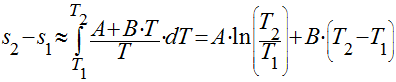
Variação da Entropia em Gases Perfeitos
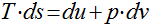
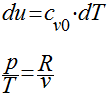
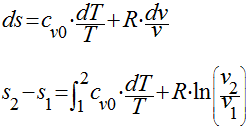
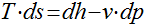
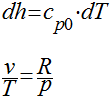
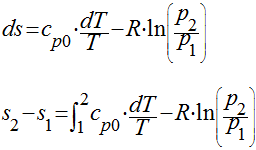
Considerar o calor específico constante
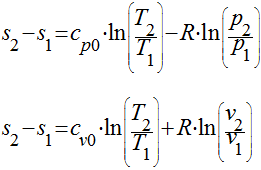
Considerar as expressões que aproximam
o comportamento do calor específico.
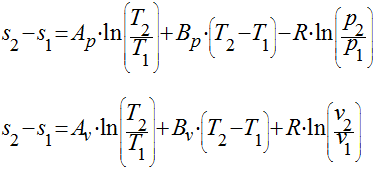
Utilizar
dados fornecidos em Tabelas para os gases reais e utilizar a seguinte expressão:
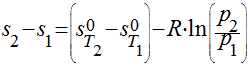
Processos Isoentrópicos
Calor Específico Constante
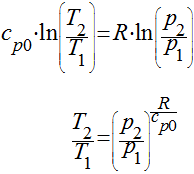
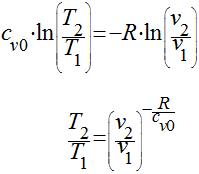
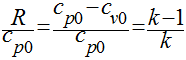
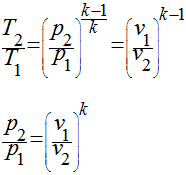
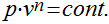
Processo Politrópico Reversível para Gases Perfeitos
Processos termodinâmicos politrópicos obedecem a seguinte relação anterior.
A expansão dos gases de combustão no cilindro de motores de combustão interna é um exemplo de processo politrópico.
O valor de n depende do tipo de processo de acordo com a Tabela abaixo.
|
Processo |
n |
Característica |
|
Isobárico |
0 |
P constante |
|
Isotérmico |
1 |
T constante |
|
Isoentrópico |
K |
S constante |
|
Isocórico |
∞ |
V constante |
Processos Irreversíveis
Finalmente, a expressão básica da entalpia para processos irreversíveis é dada por:
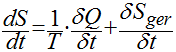
Onde:
Sger é a entalpia gerada pelo sistema devido a processos irreversíveis no interior do sistema.